Europa e mondo
Covid: via libera dell'Ema all'antivirale Paxlovid di Pfizer
24 Esclusivo per Sanità24
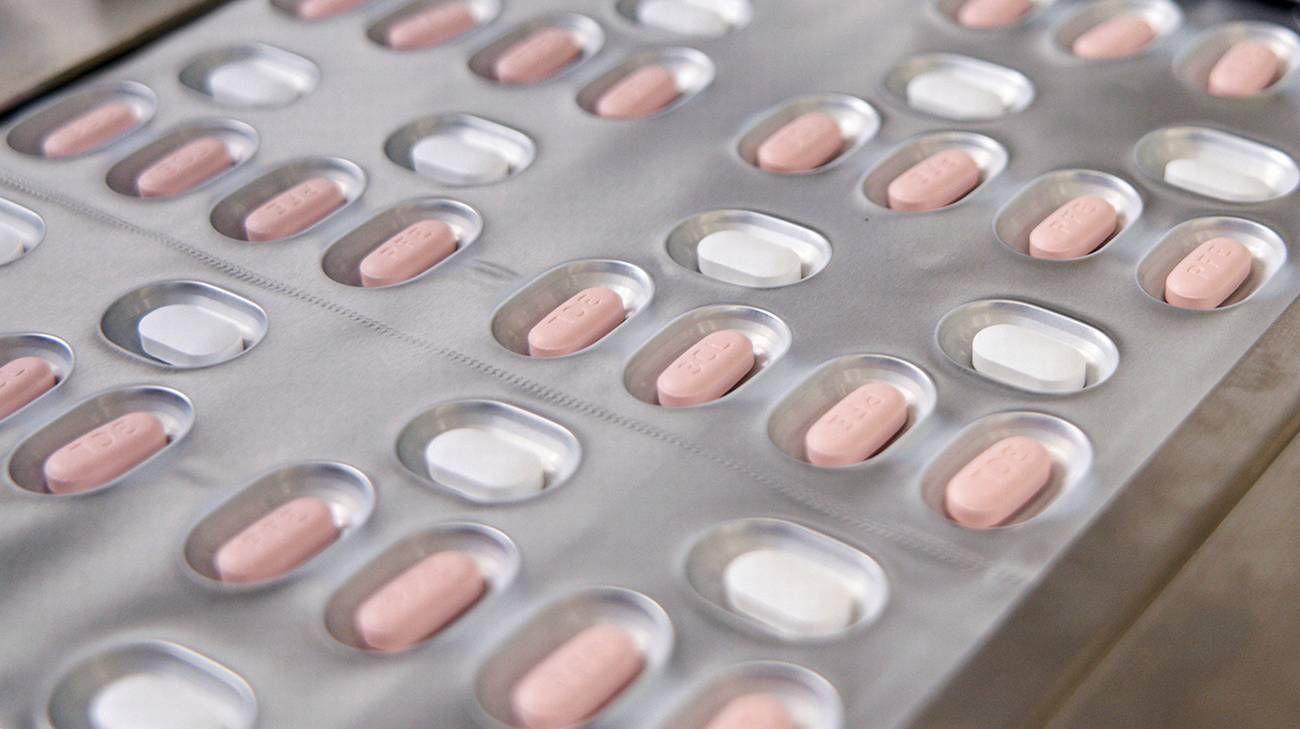
Il Comitato per i medicinali per uso umano (CHMP) dell'Ema ha raccomandato di concedere un'autorizzazione all'immissione in commercio condizionata per il medicinale antivirale orale Paxlovid (Pfizer) per il trattamento del Covid-19. L'antivirale è destinato "agli adulti che non necessitano di ossigeno supplementare e che sono ad aumentato rischio che la malattia diventi grave". Paxlovid è il primo medicinale antivirale da somministrare per via orale raccomandato nell'Ue per il trattamento del Covid-19.
Per approdare al verdetto di oggi, il Chmp ha valutato i dati di uno studio in cui il trattamento con Paxlovid ha ridotto significativamente i ricoveri o i decessi nei pazienti Covid con almeno una patologia pre-esistente che li mette a rischio di sviluppare una forma grave. Le persone arruolate nello studio hanno ricevuto Paxlovid o un placebo entro 5 giorni dall'inizio dei sintomi Covid. Nel mese successivo al trattamento, lo 0,8% (8 su 1.039) dei trattati con Paxlovid è stato ricoverato in ospedale per più di 24 ore, rispetto al 6,3% (66 su 1.046) di coloro che hanno ricevuto il placebo. Non ci sono stati decessi nel gruppo Paxlovid, mentre ce ne sono stati 9 nel gruppo placebo. La maggior parte dei pazienti coinvolti nel trial era stata infettata dalla variante Delta. Ma "sulla base di studi di laboratorio, si prevede che Paxlovid sia attivo anche contro Omicron e altre varianti", spiega l'Ema.
Il profilo di sicurezza del farmaco è stato "favorevole e gli effetti collaterali sono stati generalmente lievi. Tuttavia - aggiunge l'agenzia Ue - è noto che ritonavir influenza l'azione di molti altri medicinali" e, in considerazione di questo, sono stati "inclusi consigli e avvertenze nelle informazioni sul prodotto di Paxlovid. L'azienda ha anche fornito uno strumento sul proprio sito web a cui è possibile accedere tramite un Qr code incluso nelle informazioni sul prodotto e sulla confezione esterna". Verrà inoltre inviata "una lettera alle organizzazioni degli operatori sanitari competenti per ricordare loro ulteriormente il problema" delle interazioni con altri farmaci.
Il Chmp ha dunque concluso che i benefici del medicinale per l'uso approvato sono maggiori dei suoi rischi. Ora queste sue raccomandazioni verranno inviate alla Commissione europea per una decisione rapida applicabile in tutti gli Stati membri dell'Ue.
© RIPRODUZIONE RISERVATA

